Jumat, 25 November 2011
LAPORAN PRAKTIKUM MIKROTEKNIK
A. Tujuan:
1. Mengetahui prosedur pembuatan dan penggunaan preparat basah.
2. Mengenal dan melihat sifat juga letaknya antosianin pada Rhoeo discolor.
3. Mengetahui perubahan warna sel setelah ditetesi HCl, Haematoxylin, dan NaOH.
B. Landasan Teori
1. Pengertian Antosianin
Antosianin (bahasa Inggris: anthocyanin, dari gabungan kata Yunani: anthos = "bunga", dan cyanos = "biru") adalah pigmen yang berwarna merah sampai biru yang terlarut dalam cairan sel yang secara alami terdapat pada berbagai jenis tumbuhan. Menurut De Man (1997), pigmen antosianin terletak dalam cairan sel tumbuhan (vakuola), senyawa ini berbentuk glikosida dan menjadi penyebab warna merah, biru, dan violet. Pada dasarnya, antosianin terdapat dalam sel epidermal dari buah dan biasanya terdapat pada buah tua/masak, sayur, akar, dan daun tumbuhan hijau. Antosianin telah banyak digunakan sebagai pewarna alami pada berbagai produk pangan dan aplikasi lainnya. Antosianin merupakan sub-tipe senyawa organik dari keluarga flavonoid dan merupakan anggota kelompok senyawa yang lebih besar yaitu polifenol. Beberapa senyawa antosianin yang paling banyak ditemukan adalah pelargonidin, peonidin, sianidin, malvidin, petunidin, dan delfinidin. Pigmen antosianin terdiri dari glikogen (antosianidin) yang teresterifikasi oleh satu atau lebih gula. Antosianidin ini adalah aglikon antosianin yang terbentuk apabila antosianin dihidrolisis dengan asam. Antosianidin yang paling umum pada saat ini adalah sianidin yang berwarna merah lembayung. Warna jingga disebabkan oleh pelargonidin yang gugus hidroksilnya kurang satu dibanding sianidin, sedangkan warna merah senduduk, lembayung dan biru umumnya disebabkan oleh delfinidin yang gugus hidroksilnya lebih satu dibandingkan dengan sianidin.
Vakuola (vaccus-kosong) adalah rongga-rongga yang terbentuk di dalam lumen sel ketika sel bertambah besar dan sel bertambah tua. Berisi cairan vakuola, yaitu suatu larutan cair berbagai bahan organik dan anorganik, gula, protein, lemak, minyak, gas dan garam-garam yang kebanyakan merupakan bahan cadangan makanan atau hasil sampingan metabolisme. Vakuola ini umumnya tidak berwarna, tetapi mungkin berpigmen kebiru-biruan atau kemerah-merahan tergantung lingkungannya. Pigmen ini termasuk zat kimia kelompok antosianin dan terdapat pada bagian tumbuhan seperti akar, daun atau bunga.
2. Manfaat Antosianin
Salah satu fungsi antosianin adalah sebagai antioksidan di dalam tubuh sehingga dapat mencegah terjadinya aterosklerosis, penyakit penyumbatan pembuluh darah. Antosianain bekerja menghambat proses aterogenesis dengan mengoksidasi lemak jahat dalam tubuh, yaitu lipoprotein densitas rendah. Kemudian antosianin juga melindungi integritas sel endotel yang melapisi dinding pembuluh darah sehingga tidak terjadi kerusakan. Kerusakan sel endotel merupakan awal mula pembentukan aterosklerosis sehingga harus dihindari. Selain itu, antosianin juga merelaksasi pembuluh darah untuk mencegah aterosklerosis dan penyakit kardiovaskuler lainnya. Berbagai manfaat positif dari antosianin untuk kesehatan manusia adalah untuk melindungi lambung dari kerusakan, menghambat sel tumor, meningkatkan kemampuan penglihatan mata, serta berfungsi sebagai senyawa anti-inflamasi yang melindungi otak dari kerusakan. Selain itu, beberapa studi juga menyebutkan bahwa senyawa tersebut mampu mencegah obesitas dan diabetes, meningkatkan kemampuan memori otak dan mencegah penyakit neurologis, serta menangkal radikal bebas dalam tubuh.
3. Faktor-faktor yang memengaruhi kestabilan Antosianin
a. pH
Warna yang ditimbulkan oleh antosianin tergantung dari tingkat keasaman (pH) lingkungan sekitar sehingga pigmen ini dapat dijadikan sebagai indikator pH. Warna yang ditimbulkan adalah merah (pH 1), biru kemerahan (pH 4), ungu (pH 6), biru (pH 8), hijau (pH 12), dan kuning (pH 13). Untuk mendapatkan warna yang diinginkan, antosianin harus disimpan menggunakan larutan bufer dengan pH yang sesuai.
b. Kation
Sebagian kation, terutama kation divalen dan trivalen harus dihindari karena dapat menyebabkan perubahan warna antosianin menjadi biru hingga terjadi pengendapan pigmen. Selain itu, permukaan tembaga, baja ringan, dan besi juga sebaiknya dihindari.
c. Oksigen
Saat terlarut di dalam suatu larutan campuran, antosianin akan teroksidasi perlahan-lahan.
d. Sulfur dioksida (SO2)
Apabila sulfur dioksida bereaksi dengan antosianin maka akan terbentuk produk yang tidak berwarna. Reaksi perubahan warna tersebut bersifat reversible sehingga hanya dengan memanaskan SO2 maka warna akan kembali seperti semula.
e. Protein
Apabila sumber antosianin bereaksi dengan protein maka akan terbentuk uap atau endapan. Peristiwa ini lebih dipengaruhi oleh pigmen non fenolik yang bereaksi dengan protein seperti gelatin.
f. Enzim
Penggunaan beberapa enzim dalam pengolahan makanan yang mengandung antosianin dapat mengakibatkan kandungan antosianin di dalamnya hilang atau berkurang. Hal ini sebagian disebabkan oleh enzim glukosidase yang ada pada tahap preparasi enzim.
C. Alat dan Bahan
1. Alat :
a. Object glass
b. Cover glass
c. Kertas saring
d. Pipet
e. Alat sayat (silet)
f. Mikroskop
2. Bahan :
a. Daun Rhoeo discolor
b. Aquadest
c. Reagen HCL
d. Reagen NaOH
e. Reagen Haematoxylin
D. Langkah Kerja
1. Menyiapkan alat dan bahan.
2. Membersihkan object glass dan cover glass dengan kertas saring.
3. Menyayat setipis mungkin daun Roheo discolor dengan sayatan melintang dan membujur.
4. Meneteskan aquades pada object glass.
5. Menyimpan sayatan pada object glass, usahakan sayatan tenggelam dalam reagen.
6. Meneteskan HCl pada preparat a, NaOh pada preparat b, dan Hemaxtosilin pada preparat c.
7. Hasil sayatan di simpan pada masing-masing object glass dengan menggunakan silet.
8. Kemudian tutupi objek glass dengan cover glass, menggunakan silet.
9. Mengamati melalui mikroskop dengan pembesaran 10X – 40X.
10. Menggambar beberapa sel daun Rhoeo discolor.
E. Hasil pengamatan
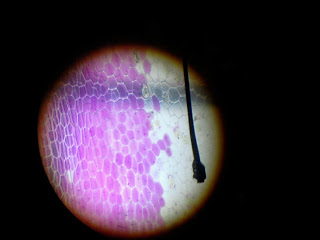
1. Sayatan Rhoeo discolor melintang
a. Sayatan Rhoeo discolor melintang dengan menggunakan reagen Aquadest + HCL
b. Sayatan Rhoeo discolor melintang dengan mengunakan reagen NaOH
c. Sayatan Rhoeo discolor melintang dengan menggunakan reagen Haematoxylin
2. Sayatan Rhoeo discolor membujur
a. Sayatan Rhoeo discolor membujur dengan menggunakan reagen Aquadest
b. Sayatan Rhoeo discolor membujur dengan menggunakan reagen Aquadest + HCL
c. Sayatan Rhoeo discolor membujur dengan menggunakan reagen NaOH
d. Sayatan Rhoeo discolor membujur dengan menggunakan reagen Haematoxylin
F. Pembahasan
Benda-benda renik tidak dapat dilihat oleh mata telanjang. Untuk melihat benda-benda tersebut tentunya kita membutuhkan alat yang dinamakan mikroskop.
Untuk mengamati sel-sel yang terdapat pada Rhoeo discolor biasanya kita menggunakan preparat basah karena untuk saat ini tumbuhan tersebut masih dapat kita jumpai di berbagai tempat. Preparat basah merupakan preparat yang paling praktis membuatannya daripada preparat awetan karena dalam pembuatan relative mudah. Akan tetapi terdapat kekurangan mengenai preparat ini yaitu penggunaannya tidak dapat digunakan dengan berulang kali. Meskipun preparat basah merupakan preparat yang praktis dalam pembuatannya, kita juga memerlukan beberapa taktik untuk mendapatkan hasil sesuai dengan yang kita inginkan, seperti sayatannya harus tipis, tidak terdapat gelembung antara reagen dan object diantara cover glass dan object glass. Juga preparat basah ini harus dijaga dengan baik supaya cover glass tidak bergerak yang mengakibatkan adanya gelembung pada object atau cover glass tersebut lepas dari object glass. Dalam pembuatan preparat diperlukan reagen yang terdiri dari berbagai macam reagen tergantung kebutuhannya . Namun pada praktikum kali ini kita menggunakan reagen Aquadest, HCl, NaOH dan Haematoxylin dan objeknya kita menggunakan daun Rhoeo discolor.
Pada praktikum kali ini, disini digunakan bahan pigmen dari epidermis bagian bawah dan atas daun Roheo discolor untuk mengetahui apakah ada perubahan antara preparat yang diberikan air, asam pekat dan basa pekat dari warna asliya. Pada kondisi awal sebelum adanya perlakuan, sel-sel Rhoeo discolor pada bagian tepinya terdapat pigmen antosianin (warna ungu) yang mengumpul pada suatu tempat. Perubahan warna pigmen terjadi ketika sayatan (object) telah ditetesi reagen. Hal ini diketahui akibat adanya sifat antosianin sangat dipengaruhi oleh pH, bila ekstrak antosianin direaksikan dengan larutan HCl (bersifat asam), pigmennya akan berubah warna menjadi warna merah muda. Sedangkan bila ekstrak antosianin direaksikan dengan larutan NaOH (bersifat basa), pigmennya akan berubah warna menjadi warna hijau yang seringkali berakhir dengan warna kuning. Terjadinya perubahan warna tersebut diakibatkan perubahan struktur antosianin akibat pengaruh ion H+ dan OH-. Sedangkan sayatan Rhoeo discolor yang direaksikan dengan reagen Haematoxylin hanya terjadi perubahan warna dan terdapat penebalan pada dindingnya, jika terdapat sel yang berwarna kuning keemasan itu berarti ekstrak tersebut mengandung lignin, akan tetapi jika tidak terdapat warna keemasan berarti ekstrak tersebut hanya mengandung sedikit lignin.
G. Kesimpulan
Dalam pembuatan preparat basah kita memerlukan cara-cara yang baik supaya mendapatkan hasil yang sesuai dengan harapan kita. Terjadinya perubahan warna pigmen pada preparat setelah ditetesi larutan diketahui akibat adanya sifat antosianin sangat dipengaruhi oleh pH. Bila ekstrak antosianin direaksikan dengan senyawa yang bersifat basa, pigmennya akan berubah warna menjadi hijau yang seringkali berakhir menjadi warna kuning. Bila ekstrak antosianin direaksikan oleh senyawa yang bersifat asam, maka ekstrak akan berubah warna menjadi warna merah muda. Bila ekstrak tersebut direaksikan dengan reagen haematoxylin akan terjadi penebalan dinding dan terdapat warna keemasanberarti ekstrak tersebut mengandung lignin. Faktor-faktor yang mempengaruhi kesetabilan adalah pH, Kation, Sulfur dioksida (SO2), Oksigen, Protein, dan Enzim.
H. DAFTAR PUSTAKA
Fita, Princess. (2011). Praktikum iv Aktivitas stomata. [Online]. Tersedia : http://princessfita.blogspot.com/2011_02_01_archive.html. [14 Februari 2011]
Mustofa, Romy Faisal. (2011). Manual Praktikum Mikroteknik. Tasikmalaya : Tidak diterbitkan.
Salisbury, F.B., Cleon W.R. 1995. Fisiologi Tumbuhan, jilid 1. Penerbit ITB, Bandung.
Sutrian, Y. (2004). Pengantar Anatomi Tumbuh-tumbuhan Tentang Sel dan Jaringan. Jakarta : PT Rineka Cipta.
Syahya, G. (2011). Letak dan Sifat Antosianin. [Online]. Tersedia : http://id.wikipedia.org/wiki/Antosianin. [23 November 2011].
Langganan:
Posting Komentar (Atom)






bagus infonya.. heheh, tolong bantuin sy dong mba..
BalasHapus